2024-2025年シーズンの日本におけるインフルエンザサーベイランスの概要
2024-2025年シーズンの日本におけるインフルエンザ流行株と抗インフルエンザ薬感受性低下株調査の概要(2026年3月6日作成)
2024年10月から2025年9月までの期間にわたり、日本各地でのインフルエンザ流行状況および薬剤耐性変異を持つインフルエンザウイルスの発生状況を調査しました。本調査では、バロキサビルに対する感受性が低下するPA遺伝子の変異、およびオセルタミビルを含むノイラミニダーゼ阻害剤に対する感受性が低下するNA遺伝子の変異を検出しました。
全国7道府県の外来医療機関が本研究に協力しました。発熱、咳、喉の痛み、だるさなど、インフルエンザが疑われる症状(インフルエンザ様疾患、ILI)がある患者のうち、迅速診断テスト(RDT)でインフルエンザA型またはB型陽性と判定された方から、上気道検体を採取し、これを初診時のサンプルとしました。また、バロキサビルを投与された患者には、3~7日後に再診をお願いし、その際に再診時の上気道検体を採取しました。これらの検体はすべて新潟大学に送付され、リアルタイムPCR(RT-PCR)法を用いてインフルエンザウイルスの検出、型/亜型の判定、PA/I38T変異の検出(A(H1N1)pdm09とA(H3N2)に対し)、NA/H275Y変異の検出(A(H1N1)pdm09に対し)を行いました。次世代シーケンシング(NGS)法とサンガー法を用いて、PA変異及びNA変異を確認しました。
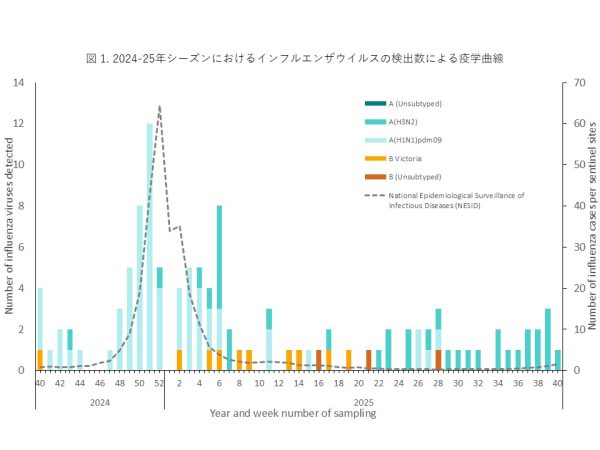
インフルエンザウイルスが検出された患者数を、検体採取日を基に週ごとに集計し、インフルエンザの疫学曲線を作成しました(図1)。
インフルエンザウイルスは2024年11月下旬(第48週)から検体数が増加し、12月下旬から1月上旬にかけてピークに達しました。流行当初からA(H1N1)pdm09が多く検出され、2024-25シーズンの流行のピークは、A(H1N1)pdm09によるものと推定されます。その後、患者数は徐々に減少し、本州では2025年4月頃(第17週)まで流行が続きました。以前は、1月から2月に流行のピークがみられましたが、新型コロナ感染症パンデミック以降、流行時期が早まっており、2024-25シーズンは年末に流行のピークが確認されました。年末年始の休診期間と流行拡大が重なったことが、特徴的な疫学的所見と考えられます。その後、A(H3N2)やB型(B/Victoria系統)が少数検出されましたが、小規模な流行にとどまりました。2025年5月以降のインフルエンザウイルスの検出は、主に沖縄におけるA(H3N2)の継続的な検出によるもので、調査期間が終了する9月下旬まで少数ながら毎月患者が確認されました。
【初診時検体】
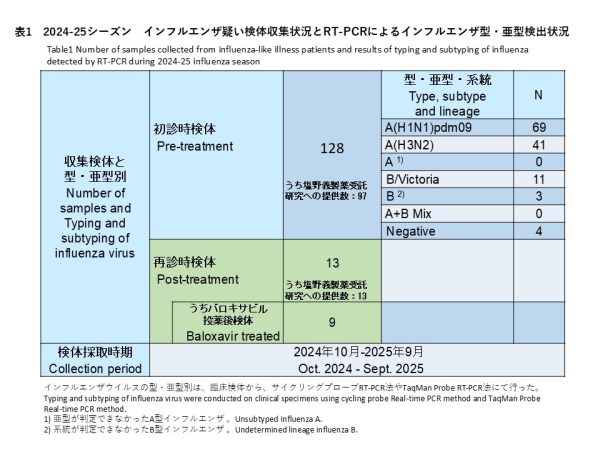
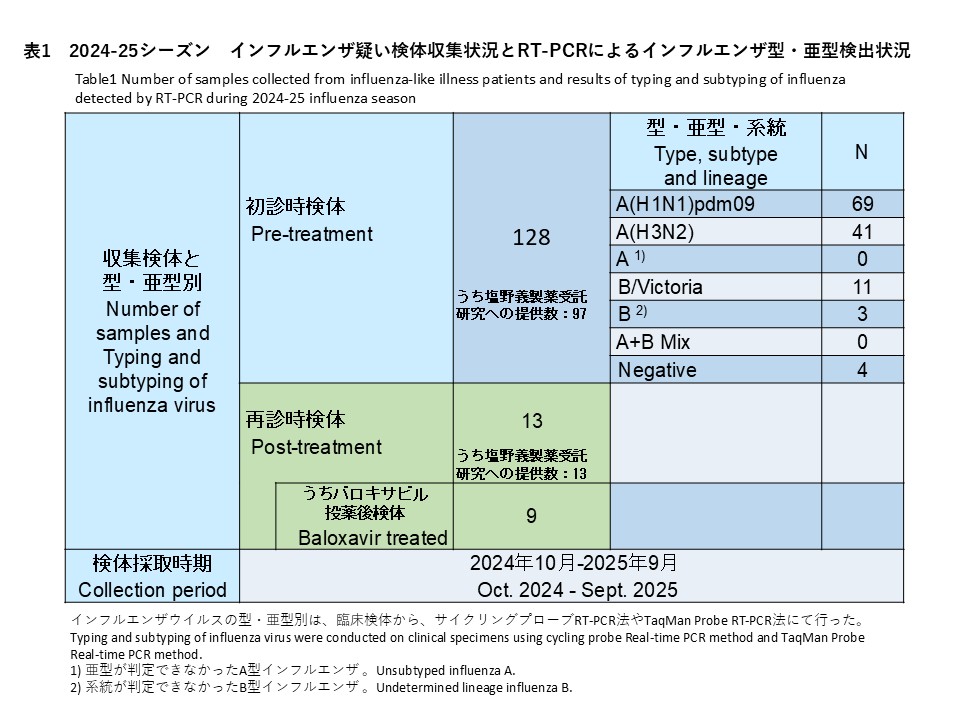
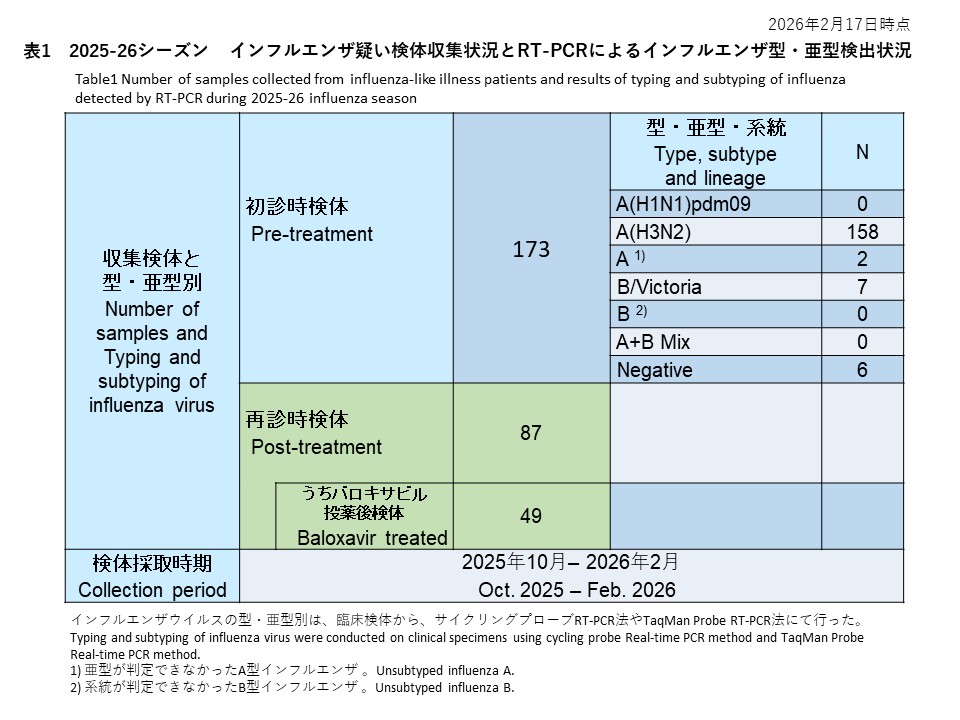
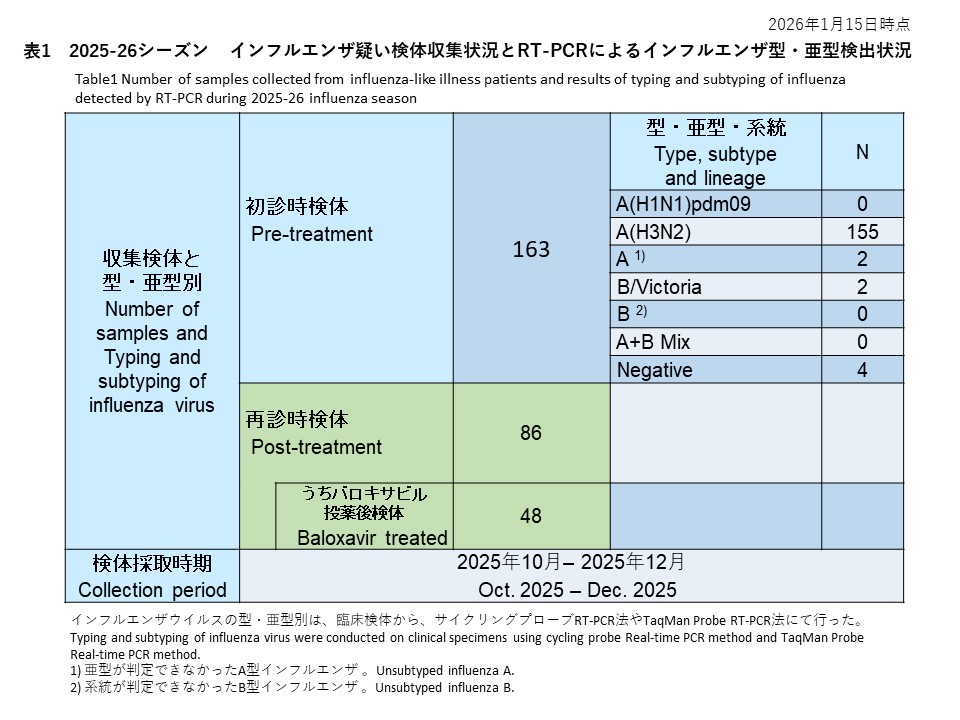
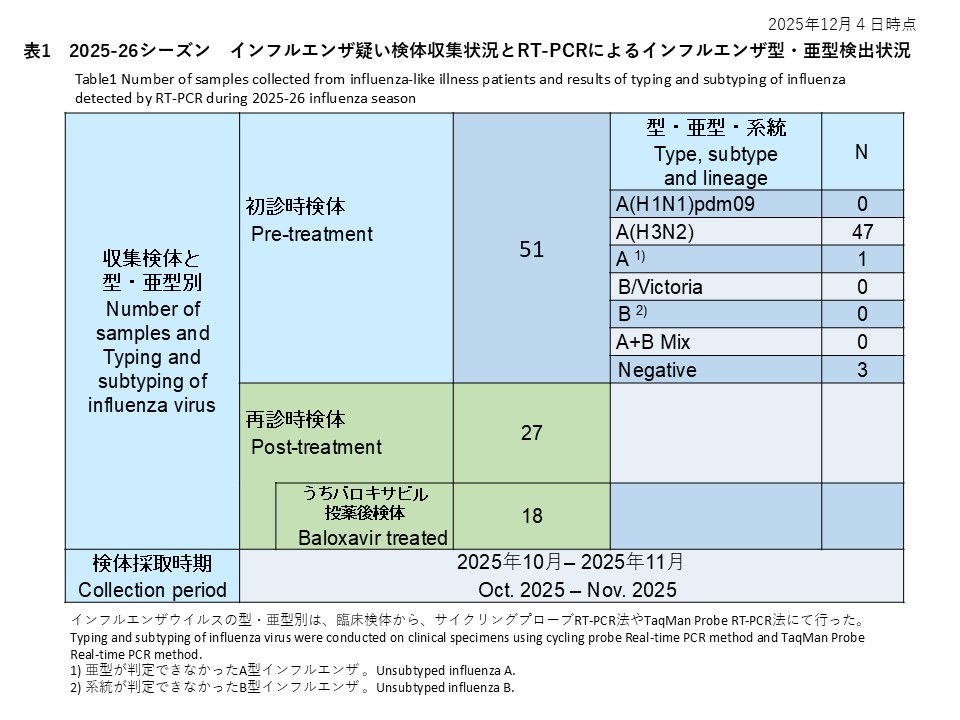
初診時に採取された128件の検体の内訳は、インフルエンザウイルスA(H1N1)pdm09が69件(53.9%)、インフルエンザウイルスA(H3N2)が41件(32.0%)、亜型判定不能のA型インフルエンザウイルスは0件(0%)、インフルエンザウイルスB/Victoriaが11件(8.6%)、系統が判定できなかったB型インフルエンザが3件(2.3%)でした。また、A型およびB型の混合感染は0件(0.0%)、RT-PCR陰性の検体は4件(3.1%)でした(表1)。
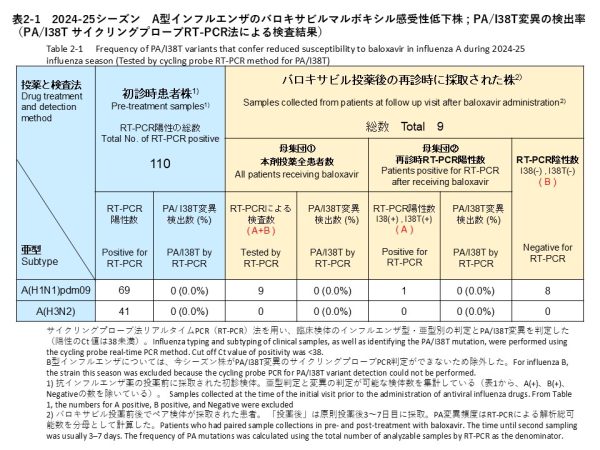
治療前に採取されたインフルエンザA型の検体について、サイクリングプローブRT-PCR法によりPA/I38T変異の検出を試みた結果、69件のA(H1N1)pdm09と41件のA(H3N2)から、PA/I38T変異陽性の検体は確認されませんでした(検出率:0%)(表2-1)。
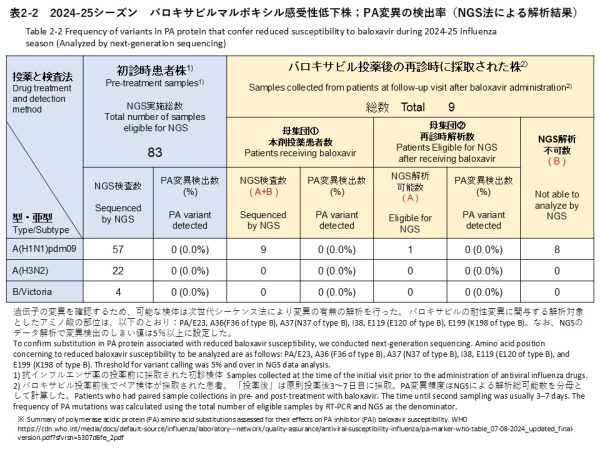
次世代シークエンス(NGS)解析によるPA変異の検出解析では、初診時検体83件のうちA(H1N1)pdm09 57件、A(H3N2) 22件、B/Victoria 4件を対象に実施しました。その結果、バロキサビル耐性に関連する変異は検出されませんでした(検出率:0%)(表2-2)。
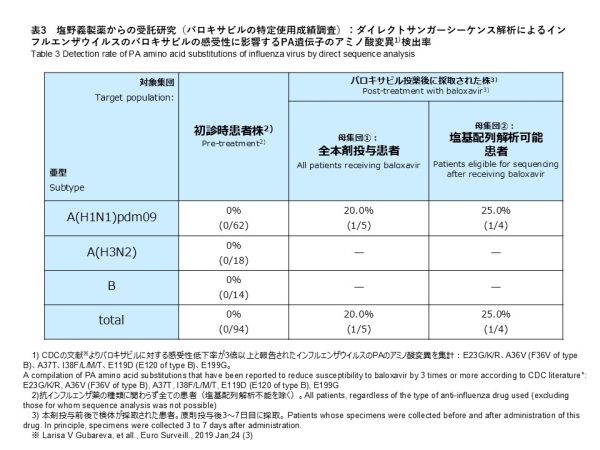
サンガー法によるPA遺伝子変異の解析では、A(H1N1)pdm09 62件、A(H3N2) 18件、B(B/Victoria、系統が判定できなかったB型インフルエンザ) 14件を対象に実施しました。その結果、バロキサビル耐性に関連する変異は検出されませんでした(検出率:0%)(表3)。
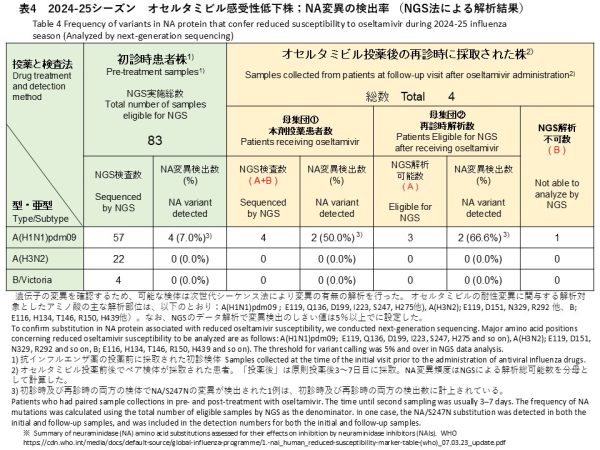
次世代シークエンス(NGS)解析によるNA変異の検出解析では、初診時検体83件のうちA(H1N1)pdm09 57件、A(H3N2) 22件、B/Victoria 4件を対象に実施しました。その結果、A(H1N1)pdm09検体からオセルタミビル耐性に関連するNA/S247N変異が1件、NA/H275Y変異が3件、計4件検出されました(検出率:7.0%)(表4)。バリアントコール解析では、これら変異の割合はいずれも99%以上であり、変異ウイルスが優勢であることが示されました。A(H3N2)およびB/Victoriaの検体では、耐性関連変異は検出されませんでした(検出率:0%)。
【再診時検体】
再診時検体は13名から採取され、9件がバロキサビル投与後、4件がオセルタミビル投与後の検体でした(表2-2、表4)。
これらの検体に対して、サイクリングプローブRT-PCR法を用いてPA/I38T変異の検出を試みた結果、PA/I38T変異陽性の検体は確認されませんでした(検出率:0%)(表2-1)。
バロキサビル投与後の再診時に採取された9件(すべてA(H1N1)pdm09)に対しNGS解析を実施し、うち1件でデータ解析が可能で、バロキサビル耐性に関連する変異は検出されませんでした(検出率:0%)(表2-2)。残りの8件は、NGSによる解析ができませんでした。
サンガー法によるPA遺伝子変異の解析では、A(H1N1)pdm09 5件を対象に実施しました。その結果、A(H1N1)pdm09 1株にI38I/F PAアミノ酸変異(Wild TypeとのMix)が確認されました(表3)。検出率は全体(5件)で20.0%、解析可能検体(4件)では25.0%でした。サンガー法により変異が検出された検体は、NGSによる解析の結果では、変異は確認されませんでした。なお、変異ありの判定は、NGS及びサンガー法の両方で変異が確認された場合としており、サンガー法によりPA変異が検出されたこの検体は、NGSによる解析では、変異は確認されませんでしたので、変異なしと総合判定しています。
オセルタミビル投与後の再診時に採取された4件(すべてA(H1N1)pdm09)に対しNGS解析を実施し、うち3件でデータ解析が可能でした(表4)。そのうち2件からNA遺伝子の変異が検出され、検出率は全体(4件)で50.0%、解析可能検体(3件)では66.6%でした。検出された変異は、初診時にNA/S247N変異が確認されていた患者の再診時検体で同変異が継続して検出されたもの(バリアントコール:99.6%)と、新たにNA/N295S変異が確認された1件(バリアントコール:18.7%)でした。
Overview of Influenza Circulating Strains and Antiviral Drug-Resistant Strains in Japan During the 2024-25 Season (As of March 6, 2026)
Between October 2024 and September 2024, we conducted a study in Japan to monitor circulating influenza strains and the emergence of antiviral resistance. The study focused on detecting substitutions in the PA gene associated with reduced susceptibility to baloxavir and substitutions in the NA gene associated with reduced susceptibility to neuraminidase inhibitors, including oseltamivir.
Participating Medical Institutions and Sample Collection
Outpatient medical institutions in seven prefectures participated in this study. Upper respiratory tract samples were collected as initial samples from patients who visited these institutions with suspected influenza symptoms (influenza-like illness, ILI), such as fever, cough, sore throat, and fatigue. These patients were confirmed positive for influenza A or B using rapid diagnostic tests (RDTs). For patients treated with baloxavir, upper respiratory tract samples were also collected during follow-up visits 3–7 days after treatment. All clinical specimens were sent to Niigata University, where real-time RT-PCR was performed for influenza virus detection, type/subtype determination, detection of the PA/I38T substitution (for A(H1N1)pdm09 and A(H3N2)), and detection of the NA/H275Y substitution (for A(H1N1)pdm09). Next-generation sequencing (NGS) and Sanger sequencing were used to confirm PA and NA substitutions.
Influenza Epidemic Curve
The number of influenza virus-positive patients was aggregated weekly based on sample collection dates to construct an epidemic curve (Figure 1). Influenza viruses were detected from late November 2024 (week 48), and the number of specimens increased thereafter, reaching a peak from late December to early January. A(H1N1)pdm09 was frequently detected from the early phase of the epidemic, suggesting that the peak of the 2024–25 season was mainly attributable to A(H1N1)pdm09. Thereafter, the number of patients gradually decreased, and in Honshu, influenza circulation persisted until approximately April 2025 (week 17).Before the COVID-19 pandemic, the seasonal peak typically occurred between January and February; however, since the pandemic, the timing of influenza epidemics has shifted earlier, and in the 2024–25 season the peak was observed at the end of the year. The overlap between the year-end and New Year holiday clinic closures and the expansion of the epidemic is considered a characteristic epidemiological finding. Subsequently, A(H3N2) and type B viruses (B/Victoria lineage) were detected in small numbers, but these remained limited to small-scale outbreaks. After May 2025, influenza virus detections were mainly due to the continued detection of A(H3N2) in Okinawa, and sporadic cases were observed monthly until the study concluded in late September.
Baseline (pre-treatment) specimens
Among 128 baseline specimens collected at the initial visit, influenza A(H1N1)pdm09 was detected in 69 specimens (53.9%), influenza A(H3N2) in 41 specimens (32.0%), unsubtyped influenza A in 0 specimens (0%), influenza B/Victoria in 11 specimens (8.6%), and influenza B with undetermined lineage in 3 specimens (2.3%). No mixed A and B infections were identified (0.0%), and 4 specimens (3.1%) were RT-PCR negative (Table 1).
For baseline pre-treatment influenza A specimens, we screened for the PA/I38T substitution using the cycling-probe RT-PCR method. No PA/I38T-positive specimens were identified among the 69 A(H1N1)pdm09 and 41 A(H3N2) specimens (detection rate: 0%) (Table 2-1).
NGS analysis for PA substitutions was performed for 83 baseline specimens, including 57 A(H1N1)pdm09, 22 A(H3N2), and 4 B/Victoria specimens. As a result, no substitutions associated with reduced susceptibility to baloxavir were detected (detection rate: 0%) (Table 2-2).
Sanger sequencing analysis of PA gene substitutions was performed for 62 A(H1N1)pdm09, 18 A(H3N2), and 14 influenza B specimens (including B/Victoria and influenza B with undetermined lineage). As a result, no substitutions associated with reduced susceptibility to baloxavir were detected (detection rate: 0%) (Table 3).
NGS analysis for NA substitutions was also performed for 83 baseline specimens, including 57 A(H1N1)pdm09, 22 A(H3N2), and 4 B/Victoria specimens. As a result, four oseltamivir resistance–associated substitutions were detected in A(H1N1)pdm09 specimens: one NA/S247N substitution and three NA/H275Y substitutions (detection rate: 7.0%) (Table 4). Variant-calling analysis showed that the frequencies of these substitutions were all ≥99%, indicating that the variant viruses were predominant in these specimens. No resistance-associated substitutions were detected in A(H3N2) or B/Victoria specimens (detection rate: 0%).
Follow-up (post-treatment) specimens
Follow-up (post-treatment) specimens were collected from 13 patients. Among them, 9 specimens were collected after baloxavir treatment and 4 specimens after oseltamivir treatment (Tables 2-2 and 4).
Using the cycling-probe RT-PCR method, we screened for the PA/I38T substitution in these specimens. As a result, no PA/I38T-positive specimens were identified (detection rate: 0%) (Table 2-1).
NGS analysis was performed for the 9 follow-up specimens collected after baloxavir treatment (all A(H1N1)pdm09). Sequencing analysis was successful in 1 specimen, and no substitutions associated with reduced susceptibility to baloxavir were detected (detection rate: 0%) (Table 2-2). The remaining 8 specimens could not be analyzed by NGS.
Sanger sequencing analysis of PA gene substitutions was performed for 5 A(H1N1)pdm09 specimens. As a result, an I38I/F PA amino acid substitution (mixed with wild-type virus) was identified in one A(H1N1)pdm09 strain (Table 3). The detection rate was 20.0% when calculated using all 5 specimens as the denominator and 25.0% when calculated using the 4 specimens for which sequence analysis was successful. The specimen in which the substitution was detected by Sanger sequencing did not show any substitution in the NGS analysis. In this study, a substitution was considered present only when confirmed by both NGS and Sanger sequencing. Therefore, this specimen was determined as having no substitution.
NGS analysis was performed for the 4 follow-up specimens collected after oseltamivir treatment (all A(H1N1)pdm09), and sequencing analysis was successful in 3 specimens (Table 4). NA gene substitutions were detected in 2 of these specimens. The detection rate was 50.0% when calculated using all 4 specimens as the denominator and 66.6% when calculated using the 3 specimens with successful sequence analysis as the denominator. The detected substitutions consisted of continued detection of the NA/S247N substitution (variant call frequency: 99.6%) in the follow-up specimen from a patient in whom this substitution had already been identified at the initial visit, and one newly detected NA/N295S substitution (variant call frequency: 18.7%).