2023–2024年シーズンの日本における季節性インフルエンザウイルスの遺伝的多様性とバロキサビル耐性変異(PA/I38T)を解析
当教室の李南君(Li Nanjun)さんを筆頭著者とする論文
“Influenza PA Substitutions and Genetic Diversity of A(H1N1)pdm09, A(H3N2), and B/Victoria Viruses in Japan During the 2023–2024 Season”
が Viruses に掲載されました。
https://doi.org/10.3390/v18010013
本研究では、2023年10月から2024年9月にかけて、日本国内1道5県・8クリニックでインフルエンザ様症状を呈した外来患者210例を対象に、季節性インフルエンザウイルス(A(H1N1)pdm09・A(H3N2)・B/Victoria)の遺伝的特徴とバロキサビル耐性変異(PA/I38T)を解析しました。次世代シーケンス(NGS)・サンガー法・サイクリングプローブRT-PCRの3手法を組み合わせ、ウイルスのクレード分類、WHOワクチン推奨株との適合性評価、および耐性変異の出現頻度を検討しました。
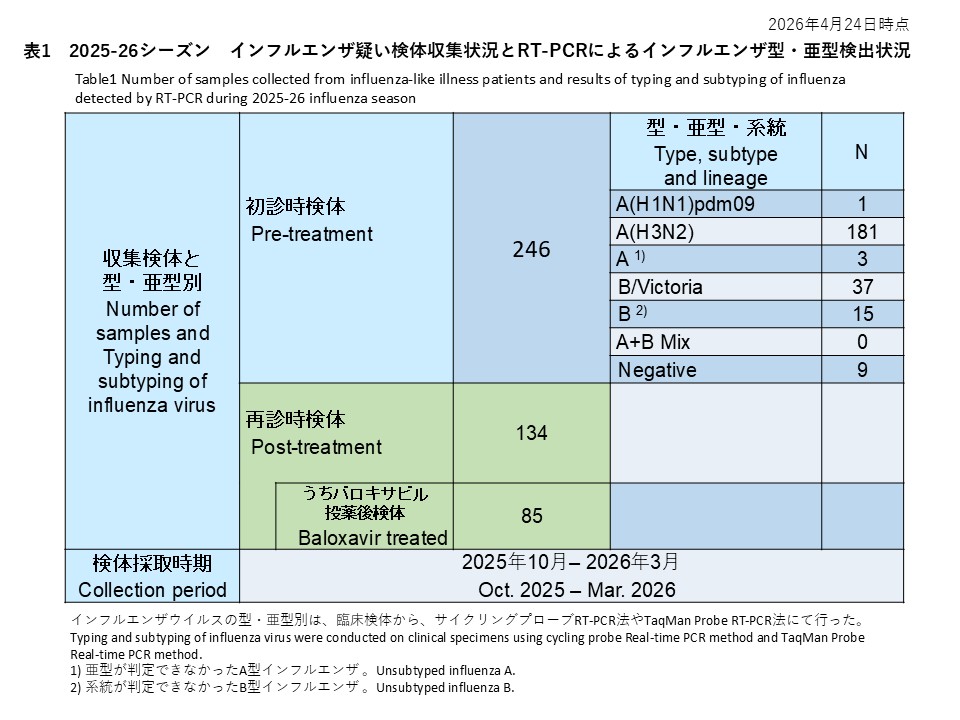
[図1] ウイルス亜型の分布と流行推移
治療前の有効検体181例のうち、A(H1N1)pdm09が44.2%(80例)、A(H3N2)が37.6%(68例)、B/Victoriaが18.2%(33例)を占めました。流行の早期(2023年11月)はA(H1N1)pdm09とA(H3N2)の混合流行で、その後2024年1月〜3月にかけてB/Victoriaが増加するという季節推移が確認されました。この流行パターンは全国サーベイランス(NESID)データとも一致していました。
A(H1N1)pdm09:ワクチン推奨株と近縁なD.2系統が優勢
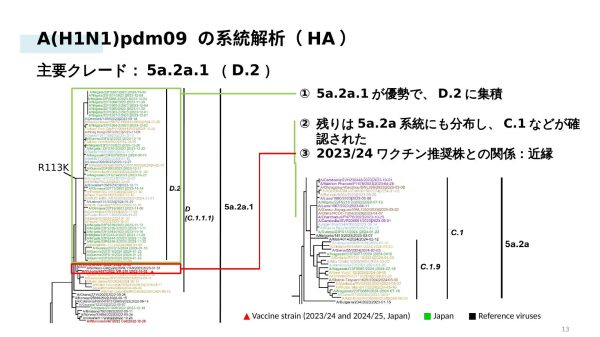
36例のNGS解析では、すべての株がクレード5a.2aまたは5a.2a.1に属し、そのうち75%(27/36例)がD.2サブクレードに集積しました。D.2は日本・中国・米国の一部で優勢な系統であり、2023/24シーズンのワクチン株(A/Victoria/4897/2022)と近縁であることが確認されました。WHOの抗原性解析データとも整合しており、H1N1pdm09成分のワクチン適合性は良好と評価されました。
A(H3N2):ワクチン株と乖離したJ系統(2a.3a.1)が全例を占める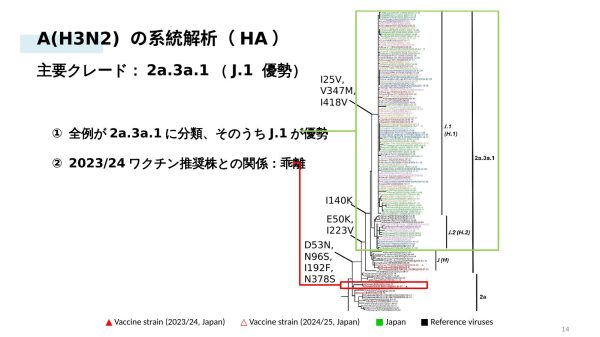
33例のNGS解析では、すべての株が2a.3a.1(J系統)に分類され、そのうちJ.1が87.8%(29/33例)を占めました。J系統は2023/24シーズンのワクチン推奨株A/Darwin/9/2021(Darwin系統)と系統的に乖離しており、抗原性の差異も報告されています。この知見は2024/25シーズンにおいてJ系統を代表するA/California/122/2022へのワクチン株更新を支持するものでした。日本で検出された株は、欧州・北米・東アジア・東南アジアの同時期の株とも混在しており、J系統がグローバルに循環していたことが示されました。
B/Victoria:V1A.3a.2(C.5系統)が世界的な動向と一致
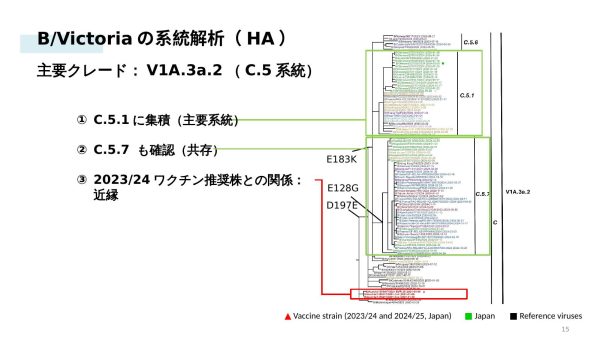
26例のNGS解析では、すべての株がV1A.3a.2のC.5バックボーン上に位置し、C.5.1(54%)とC.5.7(46%)の2つのサブクレードが確認されました。この分布は世界的な動向(C.5.1が米国・欧州の一部、C.5.7が東アジア・オーストラリア・ユーラシアで優勢)と一致しており、日本の流行も国際的な循環の一部を構成していることが示されました。2023/24シーズンのワクチン株(B/Austria/1359417/2021)はV1A.3a.2に属しており、抗原性の差異は報告されていませんでした。
バロキサビル耐性変異(PA/I38T)の検出状況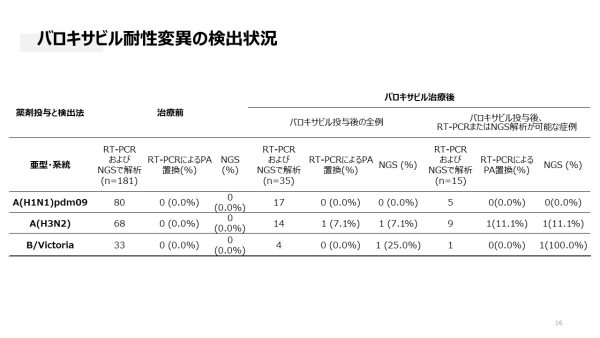
治療前検体181例すべてにおいてPA/I38T変異は検出されませんでした。この結果は、国立感染症研究所による全国サーベイランス(A(H1N1)pdm09 0.4%、A(H3N2) 0.5%、B/Victoria 0%)やWHOの集計(≤0.12%)とも整合していました。
バロキサビル治療後検体では、A(H3N2)の1例(7.1%)においてPA/I38T変異が検出され、RT-PCR・サンガー・NGSの3手法すべてで確認されました。また、B/Victoria の1例においてもNGSのみでPA/I38T変異(変異頻度25.0%)が検出されました。B型インフルエンザにおけるPA/I38T変異の臨床的検出はこれまで報告がなく、本研究が初報告に相当します。
B型インフルエンザPA/I38T検出例:家族内曝露を伴う13歳患者の経過
B/Victoria陽性で耐性変異が検出された患者2(13.3歳)は、家族内でB型インフルエンザに罹患した兄弟2人(6歳・10歳)の後に発症しました。初回受診時は迅速抗原検査陰性であったため検体採取はされませんでしたが、バロキサビルが臨床的判断で投与されました。約1週間後に再び発熱・症状が出現し、再受診時の検体にてB型インフルエンザ陽性が確認されました。この検体はウイルス量が低くRT-PCRおよびサンガー法では耐性変異を検出できませんでしたが、NGSによってPA/I38T変異が検出されました。本症例は、ウイルス量が低い検体における耐性変異の検出にNGS(次世代シークエンス)が有効であることを示す重要な知見です。
本研究の意義
本研究は、3種の検出手法を組み合わせた多層的アプローチにより、2023/24シーズンの日本における季節性インフルエンザウイルスの遺伝的特徴と抗ウイルス薬耐性の実態を明らかにしました。A(H1N1)pdm09とB/VictoriaはワクチンとHA系統的に近縁でしたが、A(H3N2)はJ系統(2a.3a.1)へのシフトによりワクチン株との乖離が生じていました。耐性変異は治療前には検出されなかったものの、バロキサビル投与後に低頻度で出現することが確認されました。特にB型インフルエンザにおける初のPA/I38T臨床検出例は、ウイルス量が低い症例での次世代シークエンスの重要性を示すものです。ワクチン株選定と抗ウイルス薬耐性の継続的な監視を統合したサーベイランス体制の重要性が改めて示されました。
論文情報
Lee N, Tang JW, Chon I, et al.
Influenza PA Substitutions and Genetic Diversity of A(H1N1)pdm09, A(H3N2), and B/Victoria Viruses in Japan During the 2023–2024 Season.
Viruses. 2026;18(1):13.
DOI: https://doi.org/10.3390/v18010013