

機能分子医学 特任教授
斎藤 亮彦
2003年に機能分子医学講座が新潟大学では初めての寄附講座として大学院医歯学総合研究科に開設された後、2007年に腎医学医療センター、2014年に病態栄養学講座の2つの寄附講座が設置されました。その後、2016年に機能分子医学講座が、2020年に病態栄養学講座が共同研究講座に移行しました。また2018年より新たな共同研究講座として生体液バイオマーカーセンター(BBC)が開設されました。
これら4つの講座は、産学連携を推進しながら、それぞれが独自の切り口から腎臓病の基礎的・臨床的問題にアプローチし、基礎的知見を臨床に応用するためのトランスレーショナルリサーチ(TR)に取り組んできました。たとえば、機能分子医学講座は主に腎臓のエンドサイトーシス受容体メガリンを基にした研究、腎医学医療センターはファブリー病に関する研究、病態栄養学講座は低タンパク質米を用いた食事療法の研究、BBCは尿中バイオマーカーの網羅的探索などを行ってきました。
昨今、TRを推進するため、レギュラトリーサイエンス(RS)の重要性が益々高まっています。RSとは「科学技術の成果を人と社会に役立てることを目的に、根拠に基づく的確な予測、評価、判断を行い、科学技術の成果を人と社会との調和の上で最も望ましい姿に調整するための科学」と定義されています(第4次科学技術基本計画2011年8月19日閣議決定)。また、2014年5月30日に制定された健康医療戦略推進法においても、RSの振興を図っていくことが国の方針として打ち出されています(独立行政法人医薬品医療機器総合機構PMDAのホームページから)。そのため2015年に、「基礎から実用化までの一貫した研究開発の推進及び環境の整備」を目的として、国立研究開発法人日本医療研究開発機構AMEDが設立されました。アンメットニーズが高く、創薬研究が遅れている腎臓病学の分野で、国策としてのTR・RSを推進することは、私たち腎臓病研究者にとって喫緊の課題です。
長年新潟大学の重要な看板のひとつであった腎研究の炎をさらに燃え立たせるため、TR部門がオリジナリティーのある優れた業績を上げていくことを目指したいと思います。

写真は、機能分子医学講座と病態栄養学講座の関係者
| 斎藤 亮彦 教授 プロフィール | |
|---|---|
| 1983年 | 旭川医科大学医学部卒業 新潟大学第2内科などで内科研修 |
| 1987年 | 国立がんセンター研究所生物学部リサーチレジデント |
| 1988-1989年 | 米国コロンビア大学遺伝学部 |
| 1990年 | 新潟大学大学院博士課程修了(医学博士号) |
| 1991年 | 信楽園病院腎センター |
| 1992-1995年 | 米国カリフォルニア大学サンディエゴ校(UCSD)分子細胞医学部門 |
| 1997-2000年 | 新潟大学腎研究施設分子病態学分野助手 |
| 2000-2003年 | 第2内科助手 |
| 2003年 | 機能分子医学講座助教授 |
| 2006年 | 同 特任教授(現在に至る) |
| 主な学会活動 | |
| 日本内科学会、日本腎臓学会、日本糖尿病学会、日本透析医学会、日本高血圧学会、病態栄養学会、アメリカ腎臓学会、国際腎臓学会 | |
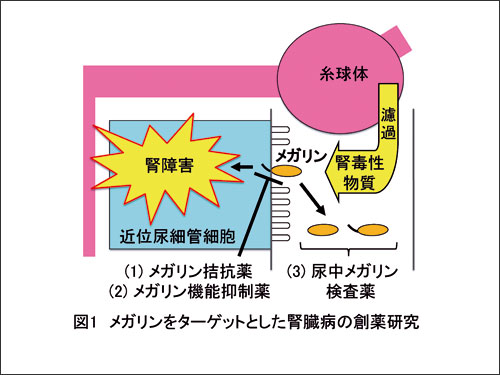
本講座は2003年度、デンカ生研株式会社の寄附講座として開設され、2016年度に親会社のデンカ(株)と新潟大学が締結した包括連携協定に基づき、2017年度より新たに同社との共同研究講座に移行しました。生体「機能分子」の研究を臨床「医学」に応用するため、開設以来、腎臓病の新しい診断・治療法の開発を目指した研究・教育を行ってきました。そのようなトランスレーショナルリサーチ(TR)に力を入れるとともに、「食と健康」というテーマに敷衍した研究や社会的活動にも取り組んできました。現在は斎藤亮彦が特任教授、後藤佐和子が特任助教を務めています。TRの重要性が注目されている状況の中で、斎藤を代表者とした研究が、2016–2018年度「メガリンを標的とした腎機能温存・再生療法の開発」、2019–2021年度「メガリンをターゲットにした急性腎障害および慢性腎臓病の創薬研究」と続けてAMEDの腎疾患実用化研究事業に採択されました。今後、メガリンを用いた腎臓病の新しい診断・治療薬の実用化(メガリン創薬)を推進したいと考えています(図1)
メガリン(megalin, LRP2)は近位尿細管の管腔側膜に発現し、糸球体を濾過する、あるいは近位尿細管細胞から分泌・放出される様々なタンパク質・ペプチド・薬剤等の再吸収・代謝に関わるエンドサイトーシス受容体であり、斎藤がUCSD留学中にクローニングしました(Saito A, et al. PNAS 1994)。これまでメガリンの機能ドメイン解析(Saito A, et al. PNAS 1996; Orlando RA, et al. PNAS 1997; Yamazaki H, et al. JASN 1998)、新規リガンドの同定(Saito A, et al. JASN 2003; Hama H, et al. Endocrinology 2004; Oyama Y, et al. Lab Invest 2005; Kaseda R, et al. BBRC 2007)、再生医学的応用モデルの開発(Saito A, et al. JASN 2003)、発現調節機構の解析(Hosojima M, et al. Endocrinology 2009; Takeyama A, et al. BBRC 2011)、細胞内アダプター分子との相互作用の解明(Hosaka K, et al. Kidney Int 2009)などを行ってきました。また、東海大学などとの共同研究によって、メガリンが腎障害において重要な役割を担うこと(Motoyoshi Y, et al. Kidney Int 2008)や、レニン-アンジオテンシン系の調節に関連すること(Matsusaka T, et al. JASN 2012; Koizumi M, et al. Hypertension 2019)を明らかにしてきました。これらの研究を経て、現在は以下の3つの創薬研究に取り組んでいます。
私たちは、メガリンが様々な腎毒性薬剤による薬剤性腎症の発症に関わるとともに、シラスタチン(腎デヒドロペプチダーゼI阻害薬)が「メガリン拮抗薬」としてそれらの腎毒性薬剤のメガリン結合を阻害することを明らかにしました(トピックス参照、特許取得 2019)。現在、この拮抗薬の臨床応用を目指し、医師主導治験に向けて準備を進めています。シラスタチンは様々な腎毒性リガンドとメガリンの結合を阻害する可能性があり、広範囲の腎疾患に適応される可能性を秘めています。我々はさらにシラスタチン以上に有効な「メガリン拮抗薬」の開発も目指しています。
肥満を伴うマウス2型糖尿病モデルにおいて、メガリンを介する腎障害機序の詳細を明らかにしました(トピックス参照)。この知見は、上記(1)とあわせ、メガリンが腎障害性物質の「入り口」を司ることを意味するとともに、過度な代謝負荷のかかるネフロンに対してメガリン機能を適度に抑制する「メガリン機能抑制薬」が有効であることを示唆しています。腎保護作用が注目されているSGLT2阻害薬などがその候補であり、現在臨床研究を進めているところです。
さらに、デンカ生研(株)と共同で尿中メガリン測定法を開発し(特許取得)、糖尿病性腎症(Ogasawara S, et al.Diabetes Care 2012; De S, et al. Diabetes 2017)やIgA腎症の重症度診断(Seki T, et al. PLoS One 2014)、小児の腎瘢痕の診断(Yamanouchi S, et al. Pediatr Res 2018)、シスプラチン腎症の発症予測(Shoji S, et al. BMC Cancer 2019)などにおける有用性を明らかにしました。現在、特定臨床検査試薬としての開発準備中です。
メガリンは肺や中枢神経系などにも発現しており、呼吸器疾患やアルツハイマー病との関連も指摘されています。今後、そのような分野の研究の発展も貢献できれば幸いです。
新潟大学農学部、亀田製菓、信楽園病院などとの共同研究として、米タンパク質が腎機能や尿酸値に与える影響について解析すると共に(Kubota M et al. Br J Nutr 2013, Hosojima M, et al. BMC Nutrition, 2016)、透析患者において高リン血症をきたさずにタンパク質摂取量を上げるための有効な供給源となることを明らかにしました(Hosojima M, et al. Sci Rep 2017)。これらの研究は、農林水産技術会議委託プロジェクト研究「農林水産物・食品の機能性等を解析・評価するための基盤技術の開発」の一環として行われ(「米タンパク質の新規生体機能調節の先導的開発と機構解析」、2011–2013年度)、このような研究活動は、後述の病態栄養学講座の設立につながりました。今後も同講座と連携して栄養学的な研究(特に腎臓とタンパク質代謝に関わる)も継続していきたいと思います。さらに新潟市と連携して、毎年、市民公開講座 新潟「食と健康」フォーラムを行っています。2020年で13回目を迎えました。

| 後藤 佐和子 特任助教 プロフィール | |
|---|---|
| 2011年3月 | 新潟大学医学部医学科卒業 |
| 2011年4月 | 山形県立中央病院 初期研修 |
| 2013年4月 | 日本海総合病院 後期研修 |
| 2014年4月 | 自治医科大学附属さいたま医療センター 臨床助教 |
| 2015年4月 | 新潟大学大学院博士課程入学(2019年3月修了, 博士号(医学)取得) |
| 2018年4月 | 新潟大学医歯学総合病院 特任助教 |
| 2019年4月 | 新潟大学機能分子医学講座 特任助教(現在に至る) |

| 細島 康宏 特任准教授 プロフィール | |
|---|---|
| 2002年3月 | 新潟大学医学部卒業 |
| 2002年4月 | 新潟大学医歯学総合病院(研修医) |
| 2003年5月 | 信楽園病院(研修医) |
| 2004年5月 | 新潟大学医歯学総合病院 第二内科医員 |
| 2005年4月 | 新潟大学大学院博士課程入学(2009年3月修了、 博士号(医学)取得) |
| 2008年7月 | 長岡赤十字病院 腎臓・膠原病内科 |
| 2010年7月 | 小千谷総合病院 内科(腎・糖尿病センター長) |
| 2012年4月 | 新潟大学農学部 農水省委託医農連携プロジェクト特任助教(新潟大学医歯学総合病院 腎・膠原病内科) |
| 2014年4月 | 病態栄養学講座 特任准教授(現在に至る) |
本講座は、腎臓病や生活習慣病などを改善させる食事・栄養療法の臨床的・基礎的研究と科学的エビデンスの構築を目的として、亀田製菓株式会社によるご寄附により、2014年4月1日付で新潟大学大学院医歯学総合研究科に設置されました。そして、2020年度からは新たに同社との共同研究講座に移行しました。担当教員は細島康宏(特任准教授)と蒲澤秀門(特任助教)で、その他数名の事務・技術補佐員から構成されています。
近年増加が著しい糖尿病、高血圧などの生活習慣病や、それらと関係の深い慢性腎臓病(CKD)に対する食事・栄養療法についての科学的エビデンスがいまだ不十分であるという背景がある中で、CKDにおける低たんぱく質食事療法の有効性に関する研究や、食事性酸負荷がCKDの進行に及ぼす影響などについて、機能分子医学講座や腎・膠原病内科と連携して、基礎的・臨床的研究を行うとともに、それらの研究に関連した教育及び社会的活動に取り組んでいます。
我々これまでに、「慢性腎臓病患者における治療用特殊食品(低タンパク質米)の使用がタンパク質摂取量に与える効果に関する多施設共同無作為化比較試験」を行ってきました。本研究は新潟県内に本社がある亀田製菓株式会社、株式会社バイオテックジャパン、ホリカフーズ株式会社、佐藤食品工業株式会社との共同研究であり、4社からの低タンパク質米の提供を受けて行われていました。さらに、平成26~28年度の新潟県の医療用途食品機能性研究事業に採択され、産官学が連携して行っている臨床研究でありました。一般的に、CKDの進行は薬物療法を始めとする現状の診療のみでは抑制することが困難なことが多く、近年、CKD患者における食事療法の重要性が見直されてきていますが、一方で、CKD患者における食事療法のエビデンスは世界的にみても不十分であり、その構築が早期に望まれています。特に、その食事療法の中心となるのはたんぱく質制限であります。しかし、長年にわたり世界的に研究され、議論されてきたにも関わらず、たんぱく質制限が腎機能低下速度を抑制するか否かについては結論が得られておらず、ガイドラインにおける推奨度は比較的、低いままであります。問題点として、これまで行われてきた臨床研究においては、示された「タンパク質摂取量」が遵守されていないものが多く、食事療法の臨床研究が極めて困難であることが挙げられます。そこで本臨床研究においては、CKD患者において推奨されるたんぱく質制限食を遂行する上で、治療用特殊食品(タンパク質米)の使用がそのアドヒアランスの向上に有効であるかについて検証しました。104人のCKD患者を対象に、4週ごとに栄養指導のみを行う群(非使用群)と、栄養指導および1日2回以上低タンパク質米を使用する群(使用群)に無作為に分けて24週間実施したところ、標準体重当たりの推定摂取タンパク質量は、使用群の方がより目標量に近づくことが分かりました。さらに低栄養や生活の質(QOL)の悪化もなく、尿蛋白も減少していることから、その腎保護効果の可能性も示唆されました(論文投稿準備中)。そこで、「慢性腎臓病患者における治療用特殊食品(低タンパク質米)の使用が腎機能低下速度に与える効果に関する多施設共同無作為化比較試験」を開始し、被験者のリクルートを積極的に行っています(図)。

また、体内の酸塩基平衡は食事の影響を受けることが知られていますが、食事に依存した酸負荷は食事性酸負荷と呼ばれ、食事摂取量の情報から算出することが可能です。最近、その食事性酸負荷が動脈硬化や糖尿病など生活習慣に起因する疾患に対して影響を及ぼす可能性が示唆されています。一方で、糖尿病性腎臓病(DKD)を含むCKDの進行において代謝性アシドーシスは独立した末期腎不全の危険因子ですが、食事性酸負荷もCKDの発症および進展に関連しているとする多くの報告が集積されつつあります。食塩やタンパク質、脂質管理などとともに、食事性酸負荷を適切に管理することが新たなCKD対策のひとつになる可能性があり、今後の更なる研究の進展が期待されていますが、日本人における詳細は明らかではありませんでした。我々は、一般住民を対象とした(新潟県)魚沼CKDコホート研究を基に、食事性酸負荷の増大が腎障害のマーカーであるアルブミン尿の増加に関連すること(Kabasawa K, Hosojima M, et al. BMC Nephrol. 2019)、さらには新潟大学医歯学総合病院に通院中のDKDを含むCKD患者を対象に、「果物」,「緑黄色野菜」,「その他の野菜」の摂取不足に関連した食事性酸負荷の増大が腎機能低下にも関わっていることを明らかにしました(Toba K, Hosojima M, Kabasawa H, et al. BMC Nephrol. 2019)。食事性酸負荷の観点からは、「野菜」や「果物」を積極的に摂取することでDKDを含めたCKDの発症および進展を抑制できる可能性があり、今後の前向きな検証を予定しています。
本講座は全国の医学部の中でも希少な、食事・栄養療法に関する新規講座として、疾患の発症機序や病態を栄養学的側面から究明し、その治療及び予防医学の発展のための研究を行っていく予定です。

| 蒲澤 秀門 特任助教 プロフィール | |
|---|---|
| 2004年3月 | 昭和大学医学部卒業 |
| 2004年4月 | 昭和大学藤が丘病院 初期臨床研修 |
| 2006年4月 | 新潟大学医歯学総合病院 第二内科医員 |
| 2007年4月 | 新潟大学大学院博士課程入学(2014年3月修了、博士号(医学)取得) |
| 2011年7月 | 新潟市民病院 腎臓・リウマチ科 |
| 2013年7月 | 長岡赤十字病院 腎臓・膠原病内科 |
| 2016年7月 | 病態栄養学講座 特任助教(現在に至る) |

| 山本 格 教授 プロフィール(写真左) | |
|---|---|
| 1974年 | 新潟大学医学部医学科 卒業 |
| 1975年 | 同医学部附属腎研究施設病理形態学部門 助手 |
| 1982年 | 同医学部附属腎研究施設病理形態学部門 助教授 |
| 1984年 | 米国スクリップス研究所免疫学部門 リサーチフェロー |
| 1999年 | 同大学院医歯学総合研究科腎研究施設構造病理学分野 教授 |
| 2004年 | 同大学院医歯学総合研究科腎研究施 施設長 |
| 2017年 | 同 名誉教授・生体液バイオマーカーセンター(BBC) 特任教授 |
| 主な学会活動 | |
| 日本腎臓学会・アメリカ腎臓学会・国際腎臓学会・日本プルテオーム学会・国際プロテオーム学会(HUPO) | |
| 平尾 嘉利 特任准教授 プロフィール(写真右) | |
|---|---|
| 2004年 | 信州大学繊維学部機能高分子学科 卒業 |
| 2006年 | 同大学院工学系研究科感性工学専攻 修了 |
| 2009年 | 東京大学大学院農学生命科学研究科応用生命工学専攻 修了 |
| 2009年 | 産業技術総合研究所糖鎖医工学研究センター 研究員 |
| 2012年 | 福井大学大学院工学系研究科ファイバーアメニティ工学 研究員 |
| 2014年 | 新潟大学産学地域連携推進機構BBC 特任助教 |
| 2017年 | 新潟大学医歯学総合研究科BBC 特任准教授 |
| 主な学会活動 | |
| 日本プルテオーム学会・国際プロテオーム学会(HUPO) | |
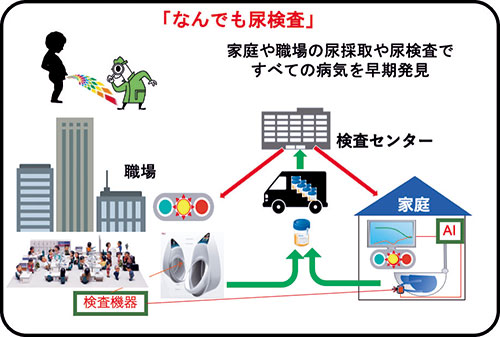
生体液バイオマーカーセンター(BBC)は2013年から「なんでも尿検査」プロジェクトを行っています。主に、尿中のタンパク質やペプチドを網羅的に解析するプロテオミクス、ペプチドミクスであらゆる病気を視野に、尿中に病気の早期発見のバイオマーカーを探索し、その検査法の社会実装することを目指しています。尿は非侵襲的に採取、検査できるので、バイオマーカーの探索、検査には大変有利な生体試料となります。
尿中には泌尿器系組織からのタンパク質のほか、血液中にあり、腎糸球体で濾過された比較的小さいタンパク質・ペプチドが排泄されて、「尿は体の鏡」とも言われています。質量分析装置で同定・定量される尿タンパク質の種類は優に1,000種類を超え、血液より多いほどです。
「なんでも尿検査」プロジェクトの最終ゴールは年数回でも家庭や職場などで尿を採取し、検査センターあるいは家庭や職場などで尿検査することで、多くの病気を早期に発見することです。それにより、重症化しないで、ほとんどの人が健康に一生を過ごせる社会を実現しようという大きな夢を追っています。
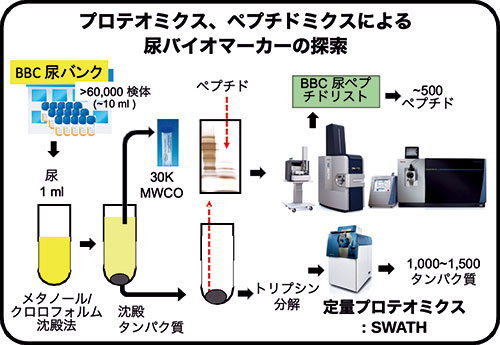
生体液バイオマーカーセンター(BBC)は2013年に東北大学の革新的イノベーション創出プログラム(COI)(JST)拠点のサテライトとしてスタートしました、2018年からは東ソー株式会社の共同研究講座として、腎臓病・糖尿病のバイオマーカー探索プロジェクトを進めています。
尿検体は主に、社会福祉法人信楽園病院や全国の病院、大学などの患者さんや医療関係者のご協力を得て集められ、現在、60,000検体以上の尿をバンキングしています。
それらの尿検体から、タンパク質とペプチドを分離し、それぞれ質量分析装置で定量解析することで、健常者、患者さんの尿中で増減しているタンパク質やペプチドを探索しています。次に、そこで選択されたタンパク質やペプチドをバイオマーカー候補として、抗体を用いた検査法を使い、より多くの検体で検証を行い、バイオマーカーを確定しています。
これまで、腎臓病尿バイオマーカーとして、腎臓部位別の組織障害バイオマーカーの探索、検証がなされました(下図)。
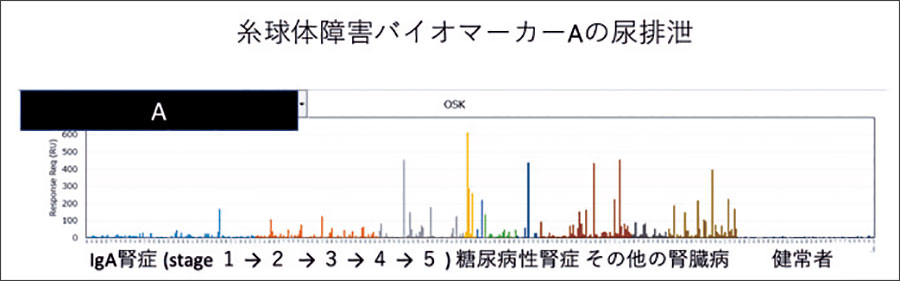
現在は、糖尿病のさまざまな臓器、組織障害を早期発見するためのバイオマーカー探索を行っています。将来は癌などのバイオマーカーも探索する予定です。
多くの方々のご支援、ご協力に深く感謝申し上げます。