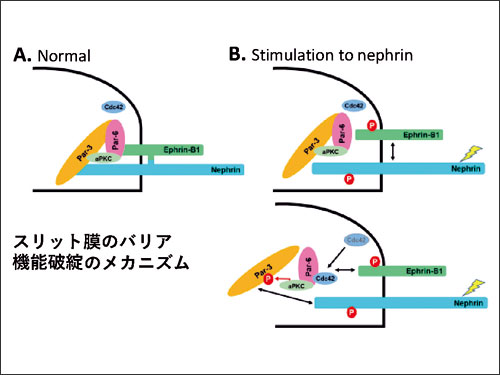
Par-3/Par-6/aPKC/Cdc42からなるPar complex (Par 複合体)は上皮系細胞の極性形成に重要な役割を果たしているとされていましたが、ポドサイトでの役割は不明でした。今回、私たちはPar-6がephrin-B1と、Par-3がNephrinの細胞質部で結合していることを明らかにしました(図A)。Nephrinが細胞外部から刺激を受けると、刺激がephrin-B1、Par-6、Par-3に伝えられ、 NephrinとPar-3、ephrin-B1とPar-6間の結合も緩み4分子複合体がバラバラになることを示しました(図B)。Par複合体がスリット膜の裏打ち部に存在し、スリット膜の構造、機能維持に重要な役割を果たしていること、Par-6のシグナル制御が新規治療法開発の戦略として重要であることを示しました。
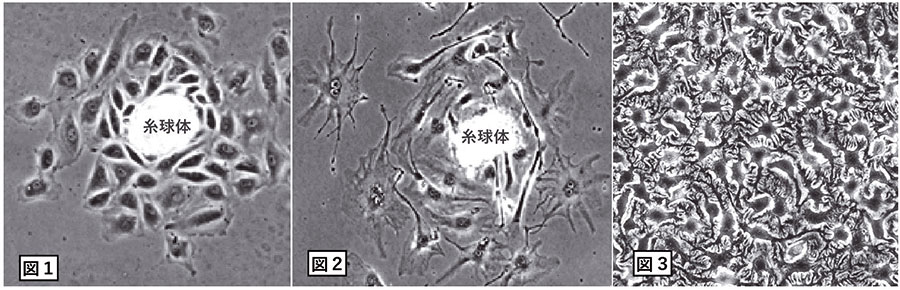
単離糸球体の培養で生えだしてくる多角形の細胞(図1)が、糸球体上皮細胞(ポドサイト)由来なのか、ボウマン嚢上皮細胞由来なのか、古くから続く問題です。多くの研究室で使われているポドサイトの細胞株は多角形細胞を基にしていますが、私たちは、従来の糸球体単離法ではポドサイトが培養初期に死滅してしまうこと、ボウマン嚢を含まない単離糸球体から多角形細胞は生えださないこと、多角形細胞と形の違う不整形細胞(図2)がポドサイトマーカーをより強く発現していること、この不整形細胞がある培養条件下で生体のポドサイトと同じ形態になること(図3)、多角形細胞をこの培養条件下で培養してもポドサイトに近似しないこと(Cell Tissue Res. 380:581-591, 2020)から、多角形細胞がボウマン嚢上皮由来であり、不整形細胞がポドサイト由来と考えています。
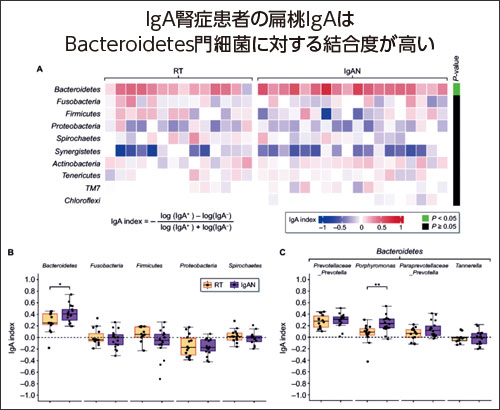
IgA腎症の発症には粘膜由来IgAの関与が想定されていますが、その詳細は不明でした。この論文ではIgA腎症患者の治療のために摘出された口蓋扁桃を用いて扁桃細菌叢に対するIgA免疫反応を解析しました。扁桃深部陰窩の組織からIgAに結合する細菌群を分離後、遺伝子解析を行い、IgA腎症患者ではBacteroidetes門細菌群に対してIgAが多く結合していることが判明しました。また、IgA腎症患者の扁桃IgA重鎖の可変領域を解析すると IGHV3-30が多く発現しており、Bacteroidetes門細菌群へのIgA結合度と有意に相関しました。IgA腎症患者の扁桃ではB細胞活性化因子が多く発現しており、特定の細菌に対するIgA免疫反応が亢進していることが病態の背景に存在すると考えられました。さらにIgA腎症患者の血液中にはBacteroidetes門細菌群に親和性を有する多量体IgAが増加しており、IgA腎症の発症に扁桃由来IgAが関与することが示唆されました。
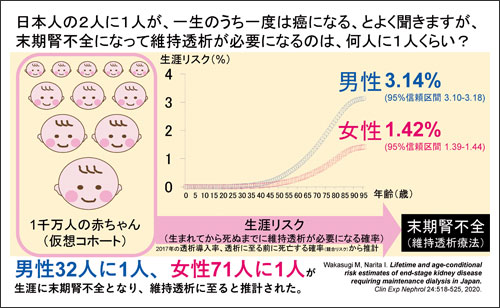
日本人の2人に1人が、一生のうちに一度は癌になる、とよく聞きますが、では、慢性腎不全になって維持透析が必要になるのは、何人に1人くらいでしょうか?透析患者は30万人強、日本の人口は1.2億強だから、400人に1人くらい?いいえ、違います、その計算では、透析に至るまでに他の疾患で亡くなる人が考慮されていません。私たちは、一般社団法人日本透析医学会の統計調査データと人口動態統計の数字を用いて、末期腎不全(維持透析)の生涯リスクを推計しました。その結果、男性の約32人に1人(3.14%)、女性は約71人に1人(1.42%)が、生涯のうちに末期腎不全に至り維持透析が必要になると推計されました。これまでわが国でこのような推計の報告はありませんでした。生涯リスクという理解しやすい数字は、CKD対策の推進に役立つことが期待されます。
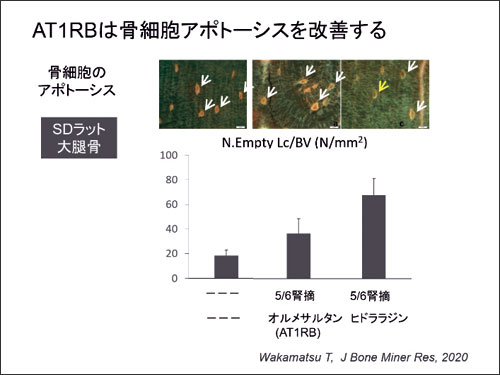
腎臓病患者、特に透析患者ではカルシウム、リン、副甲状腺ホルモンなどの異常と、骨異常、血管石灰化が起こり、臨床的に生命予後、心血管イベント、骨折が増加します。また腎臓病が進行するとレニン-アンギオテンシン系(RAS)が亢進され、降圧薬としてRAS阻害薬が頻用されます。私たちは血液透析患者でRAS阻害薬の使用は骨折の少ない発症と関連することを報告し (Yamamoto S, PLos One, 2015)、その後、病態を詳細に検討しました。腎障害を起こしたラットにRAS阻害薬であるAT1RBを使用すると骨弾性や骨組織異常の改善を認めました(図)。この結果と細胞研究、臨床研究を合わせて腎臓病患者で増悪する骨脆弱性にRASが大きく影響し、それに対しAT1RBが効果的であることを見出しました。
「米」はアジア地域の主要な穀物であり、およそ6%程度のタンパク質を含んでいます。日本人においては、肉や魚に次いで3番目、植物性タンパク質としては最も多く、この「米」からタンパク質を摂取しています。しかし、これまでにその機能性に関する検討は世界的にも、ほとんど行われてきませんでした。そのような中で、我々は亀田製菓株式会社との共同研究において、米(胚乳)タンパク質の実用化を可能にし、様々な検討を行ってきました。そして、糖尿病性腎臓病(DKD)のモデルである高脂肪食を負荷したマウスにおける検討から、幼少期からの米(胚乳)タンパク質の摂取がEscherichiaなどの腸内細菌叢の変化に関連して、その後の肥満や糖尿病およびDKDの発症および進展を抑制することを明らかにしました(Higuchi Y, Hosojima M, Kabasawa H, et al. Nutrients 2019)。特に、米(胚乳)タンパク質による腸内細菌叢への影響は、その消化物であるペプチドが関与している可能性があることも明らかにしており、今後の実用化や創薬にもつながることも期待され、更なる検討を予定しています。また、この成果は「食育」にもつながっていく可能性があり、その更なる展開も検討しています。なお、本研究の一部は、「幼少期投与用の肥満および/または肥満関連腎症予防組成物、幼少期投与用の肥満および/または肥満関連腎症予防薬、食品、並びに肥満および/または肥満関連腎症を予防する方法」として特許も出願済みです(特願2017-061684)。
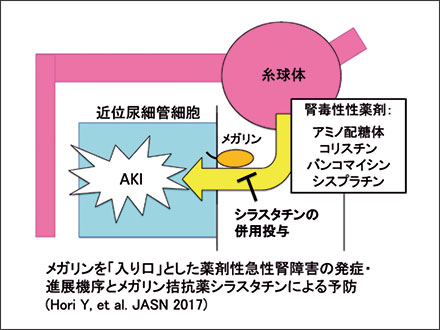
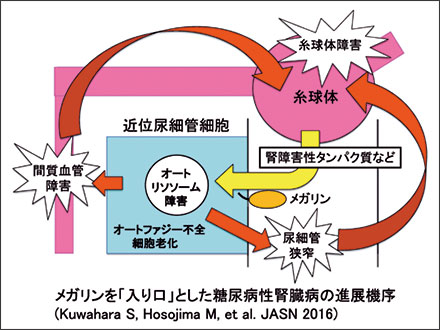
メガリンは近位尿細管腔側の刷子縁に発現し、糸球体を濾過する、あるいは近位尿細管細胞から分泌・放出される様々なタンパク質・ペプチド・薬剤等の再吸収・代謝に関わるエンドサイトーシス受容体です。我々は、メガリンがアミノ配糖体、コリスチン、バンコマイシン、シスプラチンなどの腎毒性薬剤と結合し、それらの腎取り込みによる腎障害の発症に関わるとともに、腎デヒドロペプチダーゼI阻害薬であるシラスタチンがそれらの薬剤のメガリンとの結合を阻害し、腎毒性を軽減することを見出しました (Hori Y, et al. JASN 2017; 特許取得 2019)。シラスタチンは抗菌薬イミペネムとの合剤として長年安全に使用されています。また、肥満を伴う2型糖尿病モデルである高脂肪食負荷マウスにおいて、メガリンを介する脂肪酸高含有タンパク質などの取り込みによるリソソーム障害を起点として、近位尿細管から糸球体に至る“逆行性”の腎障害が起こる機序を報告しました (Kuwahara S, Hosojima M, et al. JASN 2016)。これらの知見から、メガリンは腎毒性物質が取り込まれる「入り口」を司ることが分かりました。そこで我々は、病態に応じてメガリンの機能を適切に阻害あるいは抑制する「メガリン拮抗薬」や「メガリン機能抑制薬」、さらにそのようなメガリンの動態をアッセイする「尿中メガリン検査薬」の開発を目指しています。
山本格名誉教授はこれまでのプロテオミクスによる尿バイオマーカーの探索研究が評価され、2020年度の「HUPO2020 Clinicaland Translational Award」をアジアで初めて受賞しました。受賞対象となった内容は、尿プロテオミクスプラットフォームの構築と腎臓の障害部位別の尿バイオマーカーの確立です。前者には、HUPOイニシアチブのKidney and Urine プロジェクト(HKYPP)で作成した尿検体収集・保存ガイドと収集した尿検体からの安定したタンパク質精製法と定量プロテオミクスの確立があります。後者には、腎臓のネプロン各部の組織プロテオミクスから、新規の腎臓部位別障害尿バイオマーカーを選定し、その臨床応用をめざした研究とそれら一連の研究が「なんでも尿検査」に発展できる可能性を示したことが含まれます。
