タンパク尿発症の分子メカニズムを解明 −標的分子Cdc42を同定、新規タンパク尿治療薬開発に期待−
タンパク尿は腎臓病の最も重要な臨床症状であるだけでなく、腎臓病を進行させる最大の増悪因子です。しかし、その発症メカニズムには不明な点が多く、原因分子を標的とした有効な治療薬はありません。新潟大学大学院医歯学総合研究科腎研究センター腎分子病態学分野の河内裕教授(研究当時、現新潟大学名誉教授)、内許玉楓 (Zhang, Ying) 助教、福住好恭准教授らの研究グループは、タンパク尿発症を引き起こす細胞内シグナル伝達経路を解明し、この経路で中心的な役割を果たす分子Cdc42を同定しました。Cdc42は、新規タンパク尿治療薬の重要な標的になると考えられます。本研究成果は腎臓学分野のトップジャーナルである『Journal of the American Society of Nephrology(米国腎臓学会誌)』に掲載されました。
【本研究成果のポイント】
・腎糸球体上皮細胞(注1)の「スリット膜(注2)」はタンパク尿(血液中のタンパク質が尿に漏れ出てしまっている状態)の発症を防ぐフィルターのような構造物です。このスリット膜が細胞外からの刺激を受けると、細胞内の「Cdc42」(細胞の形や方向性を制御する重要なタンパク質)の働きが活発になることを明らかにしました。
・Cdc42が過剰に働くことで、細胞内で異常なシグナル伝達が起こり、その結果、スリット膜の構造が崩壊し、タンパク尿が発症することを明らかにしました。
・Cdc42の機能制御による新規タンパク尿治療薬の開発が期待されます。
Ⅰ.研究の背景
慢性腎臓病(注3)の総患者数は約2,000万人(成人の約5人に1人) と推定されており、「新たな国民病」として注目されています。腎臓は、生きていくための代謝で生じた老廃物を血液から濾過して尿として排泄し、一方で、身体に必要な血液中のタンパク質を尿中に漏らさないようにしています。このための濾過装置が糸球体と呼ばれる構造物です。タンパク尿は糸球体のバリア機能が低下し血液中のタンパク質が尿中に漏れ出てしまっている状態です。タンパク尿は、糸球体の傷害を示す最も重要な臨床所見であり、腎臓病を進行させる最大の増悪因子でもあることが明らかになっています。しかし、タンパク尿発症のメカニズムには不明な点が多く、タンパク尿発症の原因分子を標的とした有効な治療薬はありません。
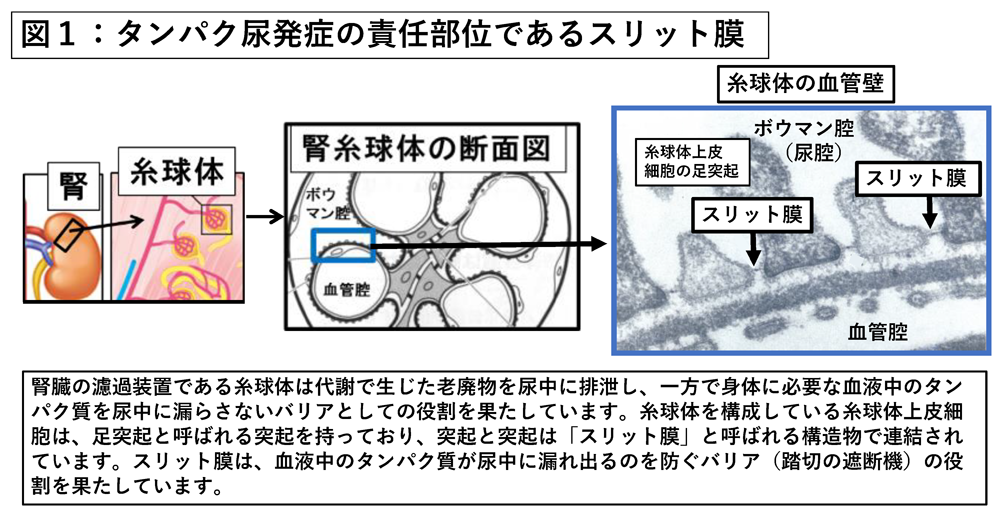
本研究グループは、世界に先駆けて、腎糸球体上皮細胞の細胞と細胞の間に存在する「スリット膜」が、タンパク尿を防ぐ最終バリアで、踏切の遮断機に相当する役割を果たしていること、タンパク尿はスリット膜のバリア機能の障害により発症することを、明らかにしました(図1)。これまでの研究で、この遮断機にはネフリン、エフリンB1、Par6と呼ばれる分子がつながって分子連結を構成し、スリット膜の機能維持に必須であることを明らかにしましたが、その生理的な意義はまだ十分に理解されていませんでした。また最近、米国、ヨーロッパの研究グループにより、重篤なタンパク尿を呈する病態であるネフローゼ症候群の多くは、ネフリンに対する自己抗体が原因であると報告されましたが、そのメカニズムの詳細は不明でした。
Ⅱ.研究の概要
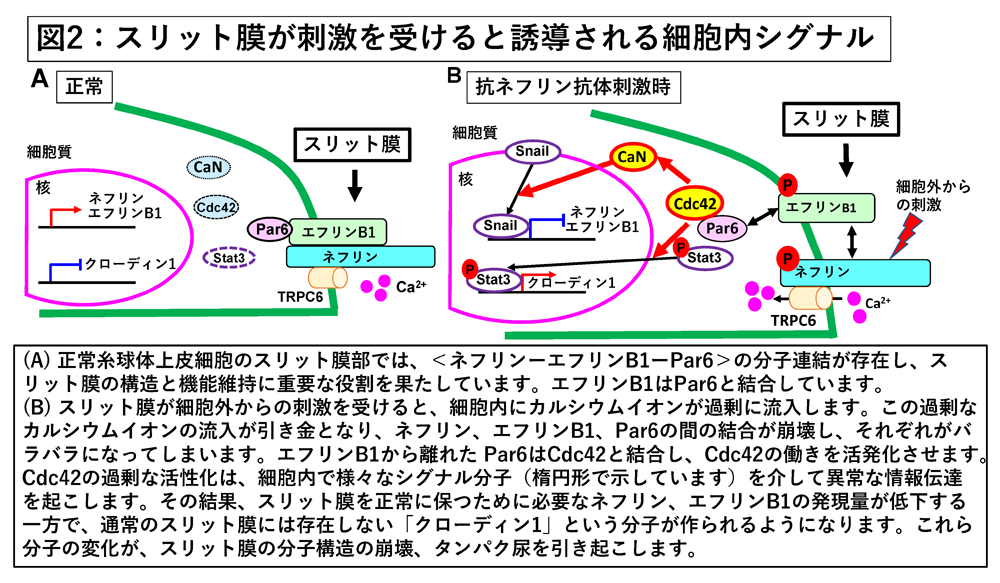
本研究では、河内裕名誉教授らは、独自に開発した抗ネフリン抗体刺激により誘導するネフローゼ症候群の動物モデル、ヒトの培養細胞を用いた検討を行い、スリット膜が抗体刺激を受けた後に細胞内で起こった異常なシグナル伝達を分子レベルで解明しました。スリット膜が刺激を受けると、細胞外から細胞内にカルシウムイオンが過剰に流れ込みます。この過剰なカルシウム流入が引き金となり、スリット膜の重要な構成分子の連結<ネフリンーエフリンB1―Par6>が崩壊し、Par6はスリット膜から離れ、Cdc42と結合することにより、Cdc42の働きを活発化させます。Cdc42の過剰な活性化が、細胞内で次々と異常なシグナル伝達を引き起こし、その結果、スリット膜を正常に保つために必要なネフリン、エフリンB1の分子の発現量が減少し、一方で、通常のスリット膜には存在しない「クローディン1」という分子が作られるようになります(図2)。これら分子の発現変化が、最終的にスリット膜の分子構造の崩壊、タンパク尿の発症を引き起こすことを明らかにしました。さらに重要な発見として、Cdc42阻害剤の投与により、ネフリンとエフリンB1の減少およびクローディン1の出現が抑制されることを明らかにしました。
Ⅲ.研究の成果
スリット膜における<ネフリン−エフリンB1−Par6>の分子連結は、スリット膜のバリア構造と機能の維持に極めて重要であり、エフリンB1がPar6を介してCdc42の過剰な働きを抑制することを明らかにしました。Cdc42の過剰な働きにより引き起こされた細胞内の異常なシグナル伝達を解明し、これはタンパク尿の発症に関わる重要なメカニズムであることを明らかにしました。
Ⅳ.今後の展開
本研究では、Cdc42の機能亢進がタンパク尿発症のキーイベントであることを明らかにしました。Cdc42の機能制御は、タンパク尿、ネフローゼ症候群の新規治療法開発のための戦略として重要であると考えます。既存薬剤、各種化合物のCdc42抑制効果の検討を進め、早急な新規タンパク尿治療薬の開発を目指します。
Ⅴ.研究成果の公表
本研究成果は、2025年6月3日、米国腎臓学会誌「Journal of the American Society of Nephrology」に掲載(出版前オンライン公開)されました。
【論文タイトル】Cdc42 Activation in Antinephrin Antibody-Induced Nephropathy
【著者】Ying Zhang*, Yoshiyasu Fukusumi*, Hidenori Yasuda, Guoqing Chang, Mutsumi Kayaba, Hiroshi Kawachi (*:両者は同等に貢献)
Department of Cell Biology, Kidney Research Center, Niigata University Graduate School of Medical and Dental Sciences, Niigata, Japan
【doi】10.1681/ASN.0000000728
Journal of the American Society of Nephrology, 2025 Jun 3. Online ahead of print.
【用語解説】
(注1)腎糸球体上皮細胞:
糸球体を構成する3種の細胞の1つで、糸球体の最外層に位置し、糸球体の形態の維持、糸球体のバリア機能の維持において最も重要な役割を果たしている細胞です。神経細胞や心筋細胞と同様、生体内で最も分化した細胞の1つで増殖能を持っていません。
(注2)スリット膜:
糸球体上皮細胞間に存在する細胞間接着装置で、タンパク尿発症の責任部位です。
(注3)慢性腎臓病:
腎の濾過機能を示す数値が60%以下になった状態、もしくは持続性のタンパク尿が確認されると慢性腎臓病と診断されます。慢性腎不全(腎機能が低下し、血液透析療法、腎移植が必要となる状態)の予備軍と考えられています。
本件に関するお問い合わせ先
【研究に関すること】
新潟大学大学院医歯学総合研究科
腎研究センター 腎分子病態学分野
名誉教授 河内 裕(かわちひろし)
助教 内許 玉楓 (うちもとかえで)
E-mail:bunshi@med.niigata-u.ac.jp
【広報担当】
新潟大学医歯学系総務課
E-mail:shomu@med.niigata-u.ac.jp