卵巣がんの抗がん剤耐性機序に関与する分子を同定 −卵巣がん患者由来の3次元培養細胞を用いた新たな解析手法に基づく成果−
新潟大学大学院医歯学総合研究科産科婦人科学分野の榎本隆之教授、同大学医歯学総合病院総合周産期母子医療センターの山脇芳助教らの研究グループは、国立がん研究センター研究所がん分化制御解析分野の岡本康司分野長らとの共同研究により、卵巣がん患者腹水中のがん細胞から作成した3次元培養細胞(スフェロイド細胞)(注1)を用いた新たな解析手法を駆使し、再発卵巣がんで問題となるプラチナ製剤に対する耐性化の機序に関与する分子を同定しました。本研究結果はElsevier社の科学雑誌Cancer Letters誌に掲載されました。
【本研究成果のポイント】
・卵巣がん患者の腹水より、3次元培養細胞である卵巣がんスフェロイド細胞を複数作成しました。
・卵巣がんスフェロイド細胞の抗がん剤感受性の違いに着目した新しい解析手法により、プラチナ製剤の耐性機序に関与する分子として、グルコース-6-リン酸脱水素酵素(G6PD)とそれに関与する一群の酸化還元酵素を同定しました。
・プラチナ製剤の一種である抗がん剤シスプラチンとG6PDの阻害剤を併用することで、プラチナ製剤への耐性を克服できることを細胞増殖実験およびマウス実験の結果より見出しました。
Ⅰ.研究の背景
卵巣がんを中心とした女性特有のがんは増加傾向にあり、我が国での卵巣がんの死亡数は増加の一途をたどっています。卵巣がんはプラチナ製剤を中心とする抗がん剤治療に対して高い効果を示すものの、多くの症例でその後に再発を認め、とくにプラチナ製剤に対して耐性を示した場合には「プラチナ抵抗性再発」として有効な治療に乏しいのが現状です。プラチナ製剤に対する耐性機序の解明と、新たな治療戦略の構築は喫緊の課題であると言えます。
Ⅱ.研究の概要
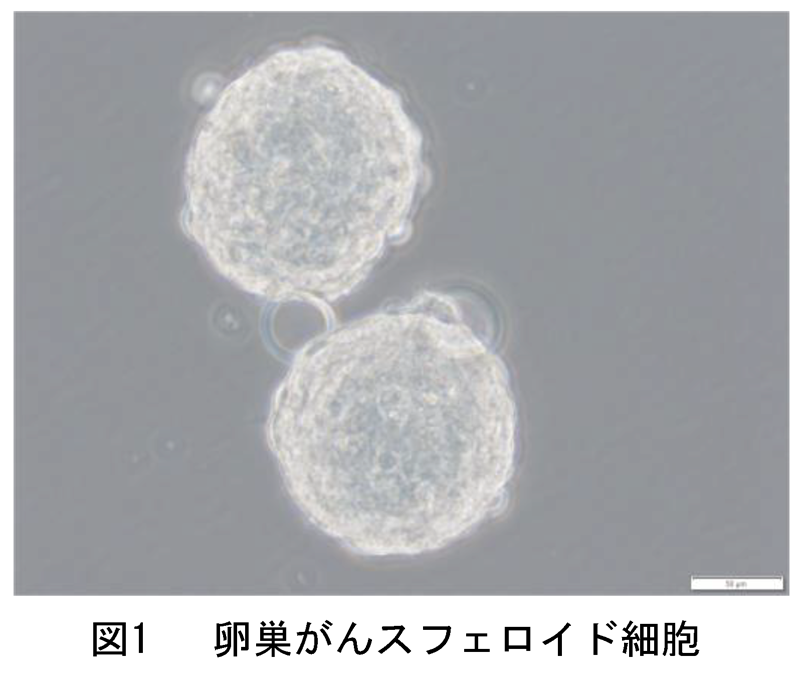
本研究グループはこれまでに、卵巣がん患者より提供いただいた腹水中のがん細胞を用いて、3次元培養細胞(注1)の一種である卵巣がんスフェロイド細胞を作成し、解析をすすめてきました(図1)。卵巣がんスフェロイド細胞は培養液中で球状の3次元構造を保って増殖をし、生体内に近い状態を保持していると考えられます。今回の研究では、新たに10種類の卵巣がんスフェロイド細胞の樹立に成功し、それらの網羅的な遺伝子発現解析と抗がん剤感受性試験を併用することで、卵巣がんの抗がん剤耐性機序に関与する分子の同定を行いました。
Ⅲ.研究の成果
樹立した卵巣がんスフェロイド細胞を用い、多種類の抗がん剤に対する感受性試験を行ったところ、プラチナ製剤への感受性が細胞によって異なることがわかりました。そこで、プラチナ製剤に対して耐性が強い細胞群と耐性が弱い細胞群に分類し、それぞれの群の遺伝子の発現を比較検討したところ、プラチナ製剤に耐性がある細胞群では、ペントースリン酸経路(注2)の律速酵素(注3)であるグルコース-6-リン酸脱水素酵素(G6PD)と、それに関与する一群の酸化還元酵素の発現が高く、それらの分子がプラチナ製剤への耐性機序に関与していることが明らかになりました。
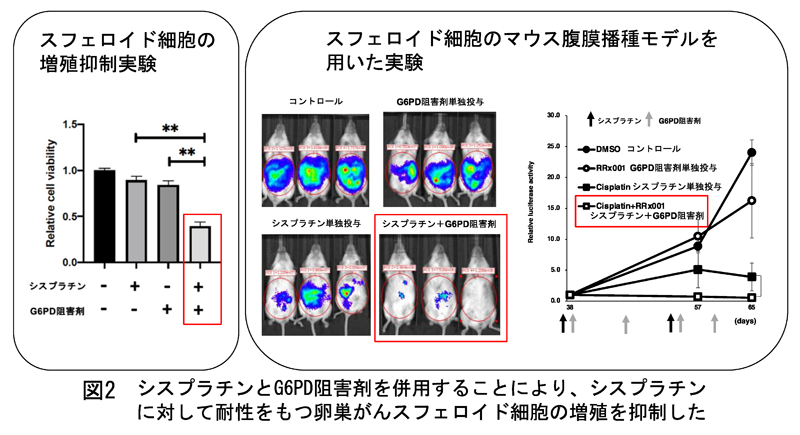
本研究では特にG6PDに着目し、スフェロイド細胞の増殖抑制実験や腹膜播種モデルを用いたマウス実験において、G6PDの阻害剤とプラチナ製剤の一種である抗がん剤シスプラチンを併用投与することで、スフェロイド細胞のもつプラチナ製剤への耐性が解除されることを見出しました(図2)。
さらに、過去に新潟大学医歯学総合病院で手術を受けた卵巣がん患者のがん組織中のG6PDの発現を確認したところ、G6PDの発現の強さと患者の予後(無増悪生存期間、全生存期間)に逆相関がみられました。
Ⅳ.今後の展開
プラチナ製剤に対して耐性が生じた卵巣がん患者にはプラチナ製剤とG6PDの阻害剤を併用することにより、プラチナ製剤の効果を回復させることができる可能性があります。また、患者由来のがんスフェロイド細胞の作成をすすめ、本研究で用いた解析手法を用いることで、他の薬剤での耐性機序に関与する分子も同定することができると考えられます。
Ⅴ.研究成果の公表
本研究成果は、2021年8月19日、Elsevier社の科学雑誌Cancer Letters誌 (Impact Factor: 8.679) のon line版に掲載されました。
論文タイトル:
Integrative analyses of gene expression and chemosensitivity of patient-derived ovarian cancer spheroids link G6PD-driven redox metabolism to cisplatin chemoresistance
著者:
Kaoru Yamawaki, Yutaro Mori, Hiroaki Sakai, Yusuke Kanda, Daisuke Shiokawa, Haruka Ueda, Tatsuya Ishiguro, Kosuke Yoshihara, Kazunori Nagasaka, Takashi Onda, Tomoyasu Kato, Tadashi Kondo, Takayuki Enomoto, Koji Okamoto
doi: 10.1016/j.canlet.2021.08.018
【用語解説】
(注1)3次元培養細胞・・・3D培養細胞とも言われ、細胞接着性の低いプレート内の培養液中やゲル中で凝集塊(スフェロイド)を形成し、生体内に近い3次元的な状態で培養される細胞のこと。スフェロイドやオルガノイドと呼ばれる3次元培養細胞が現在広くがん研究に用いられています。
(注2)ペントースリン酸経路・・・グルコースを分解しエネルギーを合成するために存在する解糖系の分岐路の1つ。本経路は細胞質においてDNA合成の原料となるリボースを生成したり、還元的生合成反応に用いられるNADPHを生成したりする役割があります。
(注3)律速酵素・・・複数の化学反応が連続しておこる一連の化学反応系において、その全体の速度を決めている段階に関わる酵素。
本件に関するお問い合わせ先
【研究内容に関すること】
新潟大学 医歯学総合病院 総合周産期母子医療センター
助教 山脇 芳(やまわき かおる)
E-mail:kymwk@med.niigata-u.ac.jp
大学院医歯学総合研究科 産科婦人科学分野
教授 榎本 隆之(えのもと たかゆき)
E-mail:enomoto@med.niigata-u.ac.jp
国立がん研究センター研究所 がん分化制御解析分野
分野長 岡本 康司(おかもと こうじ)
E-mail:kojokamo@ncc.go.jp
【広報担当】
新潟大学広報室
E-mail:pr-office@adm.niigata-u.ac.jp
国立がん研究センター 企画戦略局 広報企画室
E-mail:ncc-admin@ncc.go.jp